L’All-on-4 est devenu la référence des réhabilitations full-arch chez les patients totalement édentés ou en passe de l’être. Quatre implants, un bridge fixe, souvent posé dans la journée : la promesse est séduisante, mais la technique a des indications précises et un cadre clinique strict. Nos implantologues à Névé reçoivent régulièrement des patients qui comparent devis suisses et étrangers sans toujours comparer la même chose. Voici ce qu’un cabinet dentaire à Genève regarde vraiment avant de proposer ce protocole.
🎧 Écouter le résumé audio (1-2 min)
Key Takeaways
– Le concept All-on-4, développé par Paulo Maló à Lisbonne en 1998, utilise 4 implants (dont 2 inclinés postérieurs à 30-45°) pour supporter un bridge fixe complet d’arcade.
– Taux de survie implantaire mandibulaire ~93 % à 18 ans et survie prothétique 98,8 % — données Malo Clinic sur cohorte mandibulaire (Maló et al., 2019 — cohorte mandibulaire) ; au maxillaire, 94,7 % à 5-13 ans sur 1072 patients (Maló et al., 2019 — cohorte maxillaire).
– Indications claires : édentement complet ou dents restantes non conservables, volume osseux postérieur réduit rendant le sinus lift ou la greffe non souhaités.
– Fourchette de prix par arcade en Suisse : 22 000 à 38 000 CHF selon matériaux et laboratoire ; moins cher à l’étranger mais maintenance et reprises complexifient le calcul sur 10 ans.
L’All-on-4, c’est quoi exactement ?
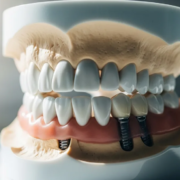
L’All-on-4 est un protocole de réhabilitation fixe complète qui utilise quatre implants par arcade pour supporter un bridge vissé — deux implants antérieurs droits, deux implants postérieurs inclinés de 30 à 45° pour contourner les structures anatomiques (sinus maxillaire, nerf alvéolaire inférieur). Cette inclinaison est la clé conceptuelle : elle permet d’ancrer l’implant dans l’os disponible sans greffe dans la majorité des cas.
Le protocole a été mis au point par le Dr Paulo Maló à Lisbonne en 1998, puis validé industriellement avec Nobel Biocare. Les données longitudinales de la Malo Clinic sont parmi les plus solides de l’implantologie full-arch : 98,8 % de survie prothétique et ~93 % de survie implantaire à 18 ans sur la cohorte mandibulaire (Maló et al., Clinical Oral Implants Research, 2019 — cohorte mandibulaire) ; 94,7 % de survie implantaire à 5-13 ans sur la cohorte maxillaire de 1072 patients (Maló et al., 2019 — cohorte maxillaire).
À ne pas confondre avec :
- Les implants unitaires multiples (6 à 8 implants par arcade, chaque couronne indépendante) — approche classique, plus coûteuse, indiquée quand l’os postérieur le permet.
- L’All-on-6 — variante avec 6 implants, souvent préférée au maxillaire édenté chez le patient jeune avec bonne densité osseuse.
- La mise en charge immédiate seule — qui désigne le fait de charger un implant le jour de la pose, indépendamment du nombre d’implants. Voir notre page mise en charge immédiate pour la distinction technique.
Pour qui l’All-on-4 est-il vraiment indiqué ?
Toutes les bouches édentées n’ont pas besoin d’un All-on-4 — et toutes ne peuvent pas en bénéficier. Les indications retenues par nos implantologues suivent les recommandations de l’European Association for Osseointegration (EAO) et de l’ITI.
Indications principales
- Édentement complet d’une ou des deux arcades, porteur de prothèse amovible insatisfaisante (douleur, mobilité, dégoût).
- Dents résiduelles non conservables (parodontite terminale, caries multiples, fractures) avec extraction planifiée.
- Résorption osseuse postérieure rendant les implants droits impossibles sans sinus lift ou latéralisation du nerf — l’inclinaison des implants postérieurs permet précisément d’éviter ces greffes lourdes.
- Refus de port de prothèse amovible (stabilité psychologique et fonctionnelle).
Contre-indications relatives à discuter en consultation
- Diabète déséquilibré (HbA1c > 8 %) — voir notre article implant dentaire et diabète.
- Tabagisme actif important — voir implant dentaire et tabac.
- Bisphosphonates IV ou antirésorbeurs osseux — voir implant et bisphosphonates.
- Hauteur osseuse inter-foraminale < 8 mm (mandibule) ou très faible densité (maxillaire postérieur sévèrement résorbé).
- Hygiène insuffisante ou patient non compliant au suivi de maintenance.
Notre lecture en cabinet. Nous refusons l’All-on-4 à un patient sur cinq qui nous consulte pour cette solution — soit parce qu’un protocole plus conservateur (2 implants + prothèse amovible stabilisée) suffira, soit parce que les conditions locales demandent un All-on-6 ou une greffe osseuse préalable. La bonne question n’est pas « puis-je avoir un All-on-4 ? » mais « quelle est la meilleure solution pour mon os et ma bouche ? ».
Les étapes d’un protocole All-on-4
Voici le déroulé que nous proposons à Névé, aligné sur les consensus ITI 2023 sur les protocoles de pose et de mise en charge (Morton et al., Clinical Oral Implants Research, 2023).
1. Bilan préopératoire (2 à 4 semaines avant)
- Examen clinique complet, analyse occlusale, photographies.
- Cone Beam (CBCT) systématique : seule la 3D donne le volume osseux, la position des nerfs, l’anatomie sinusienne.
- Empreintes optiques ou analogiques et wax-up numérique du bridge provisoire.
- Bilan biologique si terrain (diabète, anticoagulants).
- Assainissement parodontal préalable — les implants posés dans une bouche parodontalement active ont un taux de péri-implantite multiplié par 3 à 5 selon l’EFP.
2. Jour J — chirurgie et bridge provisoire
- Extractions des dents restantes si nécessaire.
- Régularisation crestale.
- Pose des 4 implants selon les axes planifiés (souvent en chirurgie guidée implantaire pour précision millimétrique).
- Si les critères de stabilité primaire sont réunis (torque d’insertion ≥ 35 Ncm, ISQ > 70), mise en charge immédiate par un bridge provisoire transvissé en résine — le patient repart avec des dents fixes le soir même dans la majorité des cas.
3. Cicatrisation (3 à 6 mois)
- Régime alimentaire mou les 4 à 6 premières semaines.
- Hygiène rigoureuse autour du bridge provisoire.
- Contrôles à 1, 3 et 6 mois.
4. Bridge définitif
- Empreintes de précision après ostéointégration complète.
- Fabrication du bridge définitif — typiquement en zircone monolithique ou titane + céramique, parfois en résine hybride renforcée pour les cas où la charge prothétique doit rester modérée.
- Pose, réglages occlusaux minutieux, contrôle radiographique.
5. Maintenance à vie
Le succès long terme dépend autant de la maintenance que de la chirurgie. Bilan et nettoyage professionnel tous les 4 à 6 mois la première année, puis tous les 6 mois — voir notre page maintenance implantaire.
Combien coûte un All-on-4 en Suisse en 2026 ?
Les honoraires dentaires suisses suivent les points TARMED/SSO, auxquels s’ajoutent les frais de laboratoire (prothèse) et le coût des implants eux-mêmes. À Genève, nos fourchettes observées en 2026 :
- Bilan + CBCT + planification : 500 à 900 CHF
- Chirurgie (4 implants + bridge provisoire mise en charge immédiate) : 12 000 à 18 000 CHF par arcade
- Bridge définitif zircone ou titane-céramique : 8 000 à 16 000 CHF selon matériau et complexité
- Extractions, régularisations, anesthésie/sédation : 1 000 à 3 000 CHF
Total par arcade : 22 000 à 38 000 CHF. Pour deux arcades (full-arch haut et bas) : 44 000 à 72 000 CHF. Pour le contexte comparatif avec les autres solutions implantaires, voir prix implant dentaire en Suisse.
Pourquoi l’écart avec l’étranger ?
Les cliniques low-cost à Budapest, Istanbul ou Tirana affichent des All-on-4 à 8 000-15 000 CHF par arcade. L’écart s’explique par les coûts salariaux, le matériel (implants génériques vs Nobel, Straumann, Astra), le nombre de contrôles inclus, et la formation des praticiens. Le risque principal que nous observons en cabinet : la reprise de complications à distance (péri-implantite, couronne qui bouge, vis de cicatrisation qui se dévisse) devient très compliquée en Suisse si les pièces prothétiques ne sont pas documentées ou compatibles.
Prise en charge par les assurances
La LAMAL ne rembourse pas l’All-on-4. Certaines complémentaires dentaires peuvent couvrir 25 à 75 % du montant, avec plafond annuel et plafond à vie. Vérifiez votre contrat avant la planification.
All-on-4 versus les alternatives : quelle solution pour votre cas ?
| Solution | Nombre d’implants | Bridge | Indication typique | Coût indicatif (par arcade, CH) |
|---|---|---|---|---|
| All-on-4 | 4 | Fixe vissé | Édentement complet, os postérieur limité | 22 000-38 000 CHF |
| All-on-6 | 6 | Fixe vissé | Os suffisant, patient jeune, occlusion forte | 26 000-42 000 CHF |
| Prothèse amovible stabilisée sur 2 implants (overdenture) | 2 | Amovible | Patient senior, budget contraint, anatomie défavorable | 8 000-14 000 CHF |
| Implants unitaires + bridges segmentés | 6 à 8 | Fixe | Os favorable partout, prothèse par secteur | 30 000-55 000 CHF |
Citation capsule. Selon le Groupe 5 du consensus ITI 2023, les protocoles de mise en charge immédiate sur arcade complète présentent des taux de survie médians de 98 % quand les critères de stabilité primaire et d’occlusion sont respectés. Morton et al., Clinical Oral Implants Research, 2023.
Les complications à connaître
Aucune technique implantaire n’est sans risque. Sur les All-on-4 suivis chez Névé, nous observons — en cohérence avec la littérature — les complications suivantes :
- Perte précoce d’un implant (< 6 mois) : 2 à 4 % des cas, souvent rattrapable par un implant de remplacement sans compromettre le bridge.
- Péri-implantite : 6 à 15 % à 10 ans — voir symptômes péri-implantite et traitement.
- Fracture prothétique (bridge provisoire ou définitif) : 5 à 10 % sur 5-10 ans, généralement réparable.
- Complications biomécaniques : dévissage de vis prothétique (réparable), fracture d’une vis (plus complexe).
- Douleur prolongée ou infection postopératoire : rare mais à signaler sans attendre — voir douleur après pose implant.
FAQ — All-on-4
Est-ce que je peux manger le soir de la pose ?
Oui, du mou et tiède. Le bridge provisoire transvissé est fonctionnel immédiatement, mais nous conseillons un régime semi-liquide pendant 48 h, puis mou pendant 4 à 6 semaines. Éviter les aliments durs, collants ou fibreux jusqu’à l’ostéointégration complète.
Combien de temps dure un All-on-4 ?
Le bridge prothétique se change typiquement tous les 10 à 15 ans (usure, décollements cosmétiques). Les implants eux-mêmes peuvent durer 20 ans et plus avec une maintenance rigoureuse — les données Malo Clinic documentent 91,9 % de survie à 18 ans. L’hygiène quotidienne et les contrôles tous les 6 mois sont non négociables.
Puis-je faire un All-on-4 si je fume ?
C’est possible mais le risque de péri-implantite et de perte précoce est significativement augmenté. Nous exigeons au minimum un arrêt 2 semaines avant et 8 semaines après la chirurgie, et recommandons fortement un arrêt définitif. Les données sont claires : le tabac divise par 2 à 3 la survie implantaire à 10 ans.
All-on-4 ou prothèse amovible : comment choisir ?
Le critère principal n’est pas le prix mais la qualité de vie. La prothèse amovible stabilisée sur 2 implants (overdenture) reste la solution la plus économique et convient à beaucoup de patients seniors. L’All-on-4 change en revanche radicalement l’expérience — manger une pomme, rire sans craindre la chute, parler sans ressentir de mouvement. Pour comparer les trois grandes options, voir implant, bridge ou prothèse.
Est-ce que c’est douloureux ?
La chirurgie se fait sous anesthésie locale, souvent complétée par une sédation consciente. Les suites opératoires sont plus marquées que pour un implant unitaire : œdème 3-5 jours, douleur modérée contrôlée par antalgiques simples pendant 48-72 h. La plupart des patients reprennent une activité normale sous 5 à 7 jours.
Puis-je faire poser mon All-on-4 à l’étranger et assurer le suivi à Genève ?
Techniquement oui, mais nous le déconseillons quand les pièces prothétiques ne sont pas clairement identifiées (marque, références). Le jour où un dévissage ou une péri-implantite survient, reprendre un système non documenté complique beaucoup la maintenance et peut renchérir le coût final au-delà de l’économie initiale.
Pour aller plus loin
L’All-on-4 est une technique mature, documentée sur près de 30 ans, qui a transformé la prise en charge de l’édentement complet. Elle n’est pas la seule réponse possible — et c’est précisément pour cela qu’une consultation implantaire sérieuse commence par un bilan 3D et une discussion ouverte de toutes les options, pas par une proposition unique.
Vous envisagez une réhabilitation complète ? Nos implantologues et parodontistes — Dr Sylvain Mouraret, Dr Paul Monneyron et Dr Spyridon Bobetsis — reçoivent à Plainpalais, Pont-Rouge et Nations pour une consultation implantaire avec CBCT et plan de traitement personnalisé. Prenez rendez-vous en ligne.
Sources clés citées :
- Maló P. et al., The All-on-4 concept for full-arch rehabilitation of the edentulous maxillae: a longitudinal study with 5-13 years of follow-up, Clinical Implant Dentistry and Related Research, 2019 (lien)
- Maló P. et al., The All-on-4 treatment concept for the rehabilitation of the completely edentulous mandible: 10 to 18 years of follow-up, Clinical Implant Dentistry and Related Research, 2019 (lien)
- Morton D. et al., Group 5 ITI Consensus Report: Implant placement and loading protocols, Clinical Oral Implants Research, 2023 (lien)
- European Association for Osseointegration (EAO) — guidelines cliniques
- Société suisse des médecins-dentistes (SSO) — sso.ch